背 景
2022年5月9日,國家藥監局發佈最新《中華人民共和國藥品管理法實施條例(修訂草案徵求意見稿)》(以下簡稱徵求意見稿),向社會公開徵求意見。現行《藥品管理法實施條例》(以下簡稱《條例》)系2002年經國務院公佈,並於2016年、2019年歷經兩次修訂。本次徵求意見稿共十章181條,與《條例》相比新增101條,以研製、註冊、生產、經營、使用爲框架。本次修訂一方面是深入推進藥品審評審批制度改革,強化藥品安全全程監管,在鼓勵創新的同時夯實持有人主體責任,專章規定了藥品上市許可持有人、藥品供應保障,包括實施藥品價格和招標採購信用評價等配套制度,另一方面也意在以法規形式鞏固2019年12月1日起施行的《藥品管理法》和《疫苗管理法》的改革成果,積累歸納散落於各通知公告、單行規定的大量補充規則與制度。本文旨在淺析徵求意見稿修訂要點,研判藥品監管新態勢,助力廣大醫藥企業在滿足監管實踐需求的前提下,保持企業自身的發展活力。

一、研製與註冊兩手都要抓,尋求創新與仿製博弈的平衡。
藥品研製與註冊作爲本次徵求意見稿新增條款條目最多的章節,相比於《條例》變化最大,意在以註冊制度創新推動研發創新,尋求藥品知識產權保護與藥品可及的平衡。本次修訂不僅吸收了2020年的《藥品註冊管理辦法》中一系列審評審批改革成果,包括建立突破性治療藥物、附條件批準上市、優先審評審批及特別審批制度等加快上市通道,也更進一步地在科技立項、融資、信貸、招標採購、支付價格、醫療保險等方面對創新予以激勵。國家也通過一系列市場獨佔期安排,激勵特定的研發導向,筆者試歸納如下: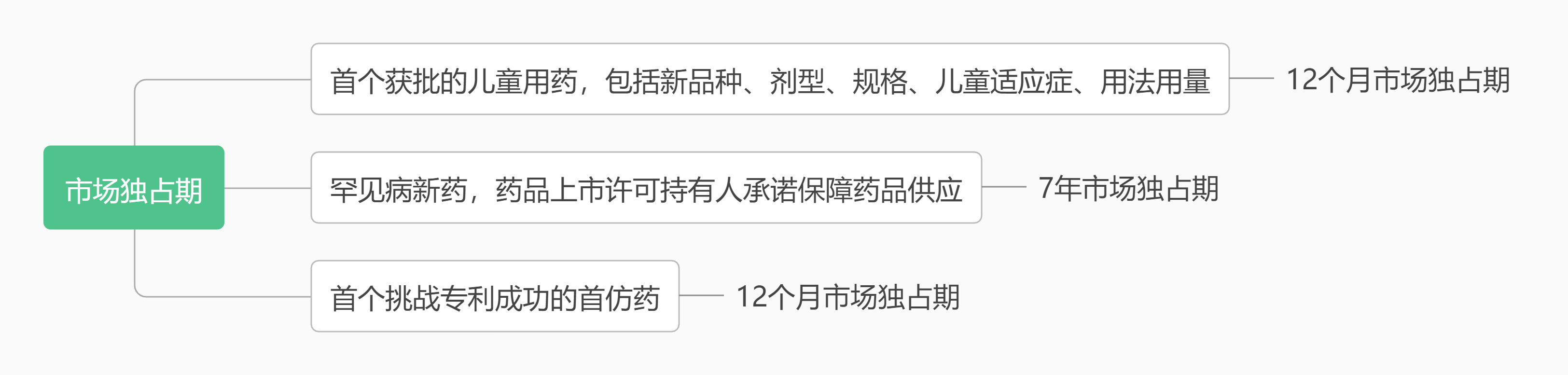
徵求意見稿第十一條、第十二條規定“國家鼓勵藥品上市許可持有人制定高於國家藥品標準的藥品註冊標準,並持續提高藥品註冊標準”、“國家實施藥品標準提高行動計劃,設立專項資金,保障藥品標準符合產業高質量發展的需要。”等內容。通過倡導性條款鼓勵從業主體持續提高藥品註冊標準這無疑能增加患者福祉,但以《藥典》收載的藥品標準爲例,如果企業提高標準後,招採環節能否產生比較優勢,提高藥品標準後的成本上升與獲益的比例以及隨之帶來的產品質量風險,均有待在醫藥行業的商業實踐中加以釐清。關於爭議解決,本次徵求意見稿不僅在第十四條強調“建立藥品註冊異議解決機制,妥善處理註冊申請人對技術審評結論的異議”,也在第三十八條銜接了此前的專利鏈接制度,筆者簡要梳理該條重點如下:②對通過技術審評的化學藥,藥監部門將根據法院生效判決、裁定或者調解書或者國務院專利行政部門行政裁決作出是否批準上市的決定;③超過一定期限未取得生效文書,藥品部門可批準藥品上市。這一藥品上市早期爭議解決機制,在審評審批環節提前介入,不僅能夠防止此前某些主體濫用訴權,造成藥品上市審評審批效率低下等情形,亦能降低仿製藥上市後專利侵權風險,也爲原研藥企業的專利佈局抑或是仿製藥企業的藥品註冊申報策略提供了有效指引。二、落實藥品上市許可持有人制度,生產經營使用全環節閉環監管。
徵求意見稿將藥品上市許可持有人專章規定,要求建立貫穿研製、生產、經營、使用等全環節的質量保證體系,並重申了對於質量管理、風險防控、責任賠償等方面的要求。對於某些監管經驗積累不夠的項目,本次修訂也提供了多個方案供業界予以討論。如MAH境內代理人的指定與變更,本次提出了兩方案:但無論最終採納何種方案,或都將終結當前某個進口產品擁有多個境內代理人的混亂情況。徵求意見稿不僅在第四十六條中規定了MAH的藥物警戒義務,亦在第四十七條規定“藥品上市許可持有人委託生產、銷售、儲存、運輸藥品及藥物警戒工作的,應當對受託方的質量保證能力和風險管理能力進行評估,與其簽訂委託協議和質量協議,並監督受託方履行有關協議約定的義務”,換言之,藥物警戒可以委託,而且或將擁有行政法規層面的依據。關於生產,本次修訂重申了對於人員、生產、物料的管理要求,同時對於委託生產、境外生產、分段生產等可能涉及到延伸檢查的事項均作出細化規定。值得一提的是,徵求意見稿新規定,註冊前規模批藥品可上市銷售,這對於單品價值較高的品規無疑是重大利好,但是其也要求質量標準、生產工藝需與註冊證書一致,相關企業可根據本前瞻性規定,合理安排生產計劃。 | |
第三條 開辦藥品生產企業,申辦人應當向擬辦企業所在地省、自治區、直轄市人民政府藥品監督管理部門提出申請。省、自治區、直轄市人民政府藥品監督管理部門應當自收到申請之日起30個工作日內,依據《藥品管理法》第八條規定的開辦條件組織驗收;驗收合格的,發給《藥品生產許可證》。
|
第五十二條【生產許可】 從事藥品生產活動,應當向所在地省、自治區、直轄市人民政府藥品監督管理部門申請生產許可,並按照國務院藥品監督管理部門規定,提交其符合《藥品管理法》第四十二條規定條件的資料。省、自治區、直轄市人民政府藥品監督管理部門應當自受理申請之日起30個工作日內作出決定。
省、自治區、直轄市人民政府藥品監督管理部門組織開展技術審查和評定、現場檢查,對符合規定條件的,準予許可並發給藥品生產許可證;對不符合規定條件的,不予許可並書面說明理由。技術審查和評定、現場檢查、企業整改等所需時間不計入期限。
新建疫苗生產企業的,應當由省、自治區、直轄市人民政府工業和信息化主管部門依據國家疫苗行業發展規劃和產業政策進行審查。經審查同意後,按規定申請藥品生產許可。
|
|
第六十條【註冊前規模批藥品上市銷售】 質量標準、生產工藝與註冊證書一致的商業規模批次藥品,其生產過程符合藥品生產質量管理規範的,在取得藥品註冊證書後,符合產品放行要求的,可以上市銷售;藥品上市許可持有人應當對其加強生產銷售管理和風險管理。
|
關於經營,本次修訂除了藥品經營許可等程序性事項,也強調了對於藥品零售的從嚴管理,包括處方藥不得開架銷售、藥品零售連鎖經營總部不得對外銷售藥品,藥品零售連鎖門店不得從所屬藥品零售連鎖總部以外的單位購進藥品等,同時對於運輸配送也提供了多個備選方案供業界予以討論。值得一提的是,徵求意見稿新納入了對於藥品網絡銷售管理的若幹條款,包括上市許可持有人的義務、第三方平臺管理義務、藥品網絡零售的處方管理,其無疑透露出監管部門對於“線上線下同要求、藥品流通環節無死角”的閉環監管態度。 | |
第十一條 開辦藥品批發企業,申辦人應當向擬辦企業所在地省、自治區、直轄市人民政府藥品監督管理部門提出申請。省、自治區、直轄市人民政府藥品監督管理部門應當自收到申請之日起30個工作日內,依據國務院藥品監督管理部門規定的設置標準作出是否同意籌建的決定。申辦人完成擬辦企業籌建後,應當向原審批部門申請驗收。原審批部門應當自收到申請之日起30個工作日內,依據《藥品管理法》第十五條規定的開辦條件組織驗收;符合條件的,發給《藥品經營許可證》。
第十二條 開辦藥品零售企業,申辦人應當向擬辦企業所在地設區的市級藥品監督管理機構或者省、自治區、直轄市人民政府藥品監督管理部門直接設置的縣級藥品監督管理機構提出申請。受理申請的藥品監督管理機構應當自收到申請之日起30個工作日內,依據國務院藥品監督管理部門的規定,結合當地常住人口數量、地域、交通狀況和實際需要進行審查,作出是否同意籌建的決定。申辦人完成擬辦企業籌建後,應當向原審批機構申請驗收。原審批機構應當自收到申請之日起15個工作日內,依據《藥品管理法》第十五條規定的開辦條件組織驗收;符合條件的,發給《藥品經營許可證》。
| 第七十條【經營許可】 從事藥品批發活動,應當向所在地省、自治區、直轄市人民政府藥品監督管理部門申請經營許可,並按照國務院藥品監督管理部門規定,提交其符合《藥品管理法》第五十二條規定條件的資料。省、自治區、直轄市人民政府藥品監督管理部門應當自受理申請之日起20個工作日內作出決定。
從事藥品零售活動,應當向所在地設區的市級人民政府藥品監督管理部門或者縣級人民政府藥品監督管理部門申請經營許可,並按照國務院藥品監督管理部門規定,提交其符合《藥品管理法》第五十二條規定條件的資料。藥品監督管理部門應當自受理申請之日起20個工作日內作出決定。
受理申請的藥品監督管理部門組織開展技術審查、現場檢查,對符合規定條件的,準予許可並發給藥品經營許可證;對不符合規定條件的,不予許可並書面說明理由。技術審查、現場檢查、企業整改等所需時間不計入期限。
從事藥品零售連鎖經營活動的企業總部,應當按照本條第一款的規定,取得藥品經營許可證。 |
|
第八十二條【藥品網絡銷售管理】 從事藥品網絡銷售活動的主體應當是依法設立的藥品上市許可持有人或者藥品經營企業,銷售的藥品應當是藥品上市許可持有人持有的品種或者是藥品經營企業許可經營的品種。
從事藥品網絡銷售活動應當符合藥品經營質量管理規範要求,藥品銷售、儲存、配送、質量控制等有關記錄應當完整準確,不得編造和篡改。
第八十三條【第三方平臺管理義務】 藥品網絡交易第三方平臺提供者應當向所在地省、自治區、直轄市人民政府藥品監督管理部門備案,未經備案不得提供藥品網絡銷售相關服務。
第三方平臺提供者應當建立藥品網絡銷售質量管理體系,設置專門機構,並配備藥學技術人員等相關專業人員,建立並實施藥品質量管理、配送管理等制度。第三方平臺提供者不得直接參與藥品網絡銷售活動。
第三方平臺提供者應當對入駐的藥品上市許可持有人、藥品經營企業資質進行審查,對發佈的藥品信息進行檢查,對交易行爲進行管理,並保存藥品展示和交易管理信息。發現藥品交易行爲存在問題的,應當及時主動制止,涉及藥品質量安全的重大問題的,應當及時報告藥品監督管理部門。
第八十四條【藥品網絡零售管理】 藥品零售企業通過網絡銷售處方藥的,應當確保處方來源真實、可靠,並經審覈後方可調配。對於未通過處方審覈的,不得直接展示處方藥的包裝、標籤、說明書等信息。
國家實行特殊管理以及用藥風險較高的藥品不得通過網絡零售,具體目錄由國務院藥品監督管理部門制定。
|
除此之外,徵求意見稿對中藥材、中藥飲片的生產、加工炮製、標籤包材等均作了有關規定。在使用環節,也即醫療機構藥事管理,本次修訂在醫療機構製劑管理、處方外流、同情用藥、藥物緊急使用等方面均加以規定,上述內容業界討論良多,限於篇幅筆者不再贅述。三、將集採進行到底,藥品招採路在何方。
長時間以來醫藥領域商業賄賂、不正當競爭等行爲頻發,造成藥品價格虛高、醫保基金流失等問題。本次徵求意見稿回應行業形勢,新增“藥品供應保障”一節以確保藥品的可及性,其中增設了合理招採價格監測、實施藥品價格和招標採購信用評價、捐贈藥品管理等規定,這不僅表明國家要將集採進行到底的態度,也體現了招採信用評價將成爲政府間接調整藥品價格、促進市場公平競爭的重要手段。筆者將徵求意見稿中將對招採環節產生影響的條款梳理如下:第一百二十五條【合理招採價格監測】 醫療保障部門集中帶量採購藥品應當堅持需求導向、質量優先原則,以市場爲主導合理確定藥品價格,建立健全藥品價格監測體系,開展藥品價格成本調查,實施藥品價格和招標採購信用評價,健全價格調整和退出機制,保障藥品質量和供應。自18年醫保局帶量採購後集採逐漸常態化,各省份均已建成省級藥品招採平臺,其主要職能爲集採、數據管理、監管協助、投訴調查等。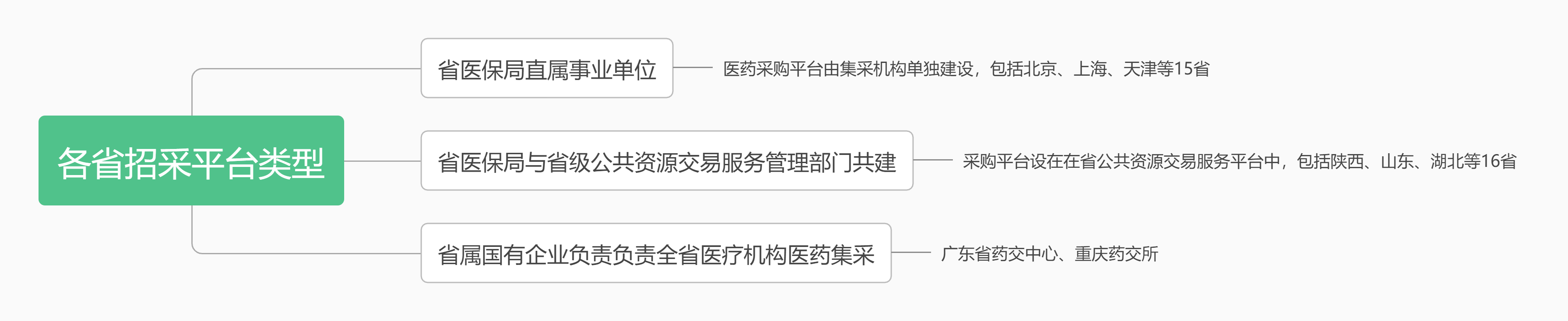
本條中提到的若幹職能,在實踐中往往由省級招採平臺行使,這也預示着省級招採平臺的功能或將與國家相關機構的職能進一步靠攏,相關從業者需對平臺職能和議事規則等深刻理解,方能在各類招採中有的放矢,反之則極易在實踐中產生爭議。本條中還重申了招採信用評價制度,早在2020年,醫保局業已發佈了相關文件,通過將醫藥企業在履約過程中,通過賄賂、涉稅違法、不正當價格行爲等失信事項納入醫藥價格和招採信用評價範圍,並將企業信用分級按“一般、中等、嚴重、特別嚴重”分級處置,同時亦賦予企業信用修復等救濟措施。125條中規定的若幹組合拳繁複,醫藥企業需結合自身業務開展情況,掌握招採規則體系,方能在“騰籠換鳥”的集採大潮中做到合規,避免因爲對於規則體系的誤讀而陷入價格持續降低的漩渦中。此外,徵求意見稿第五十一條規定“藥品上市許可轉讓同一品種不同規格的,所有規格應當一次性變更爲同一藥品上市許可持有人。”,該條文是對目前業內普遍存在的批文流轉行爲的否定性評價,如一旦通過或將對擁有多品規的企業在招標準入中擁有不利影響。結 語
整體而言,徵求意見稿不僅將當前散落於各部門規章、通知公告、單行規定的各種補充規則集於一身,也貫徹了《藥品管理法》、《疫苗管理法》的穿透監管、閉環監管的立法精神,用註冊制度激勵創新的同時亦鼓勵專利挑戰,在醫保談判的同時亦將集採進行到底,如何在左右互搏中最終提高患者福祉,我們期待監管機構貢獻的中國智慧。



